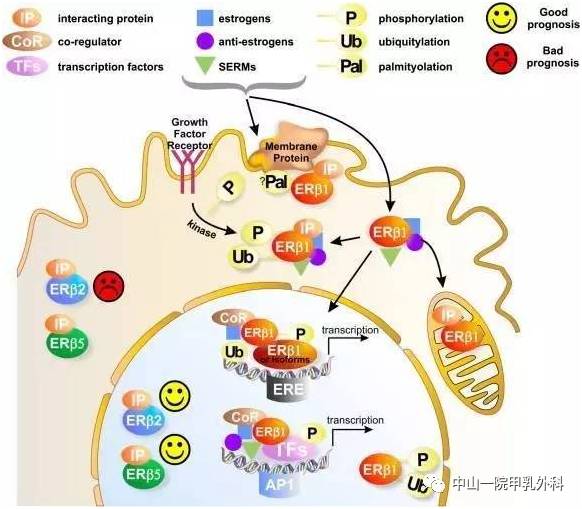
近年来,我国乳腺癌的发病率越来越高,而且呈年轻化发展的趋势。乳腺癌患者中,大概有2/3的人雌激素受体是过表达的,属于激素依赖性肿瘤,这部分病人能够通过内分泌治疗获益。因此,内分泌治疗在乳腺癌治疗中有着重要的地位和作用。目前,乳腺癌内分泌治疗涉及的药物种类繁多,机制也各不相同。今天,小编为大家盘点一下乳腺癌常用的内分泌治疗药物。 代表药物:Tamoxifen/ target=_blank class=infotextkey>他莫昔芬(TAM)、托瑞米芬、雷洛昔芬 作用机制:结构类似雌激素,能与雌二醇竞争胞内雌激素受体,与受体形成稳定的复合物并转运于核内,使胞内雌激素受体被耗竭,阻断雌二醇体内吸收,从而抑制雌激素依赖性的乳腺癌生长。 他莫昔芬于1971年首次应用于临床,于1978年在美国FDA批准用于乳腺癌,已经有近60年的使用历史。他莫昔芬适用于各期的乳腺癌,包括绝经前后的乳腺癌都可以使用。药物总体治疗乳腺癌的有效率大概在30%,能够预防大部分ER阳性乳腺癌的进展。他莫昔芬具有部分的雌激素受体激活作用,可对子宫内膜产生影响,可能的病理变化包括子宫内膜息肉样增生、子宫内膜息肉、子宫内膜不典型增生、子宫内膜癌。他莫昔芬的副作用包括潮热、恶心、体液潴留、子宫内膜增厚、子宫肌瘤、皮疹、疲劳、阴道出血、胃肠不适、头痛、头晕等。有肺栓塞史及深静脉血栓形成史的患者禁用 TAM。 主要用在绝经后雌激素受体阳性的患者,同样适用于早期和晚期雌激素阳性的乳腺癌患者。该药与 ER 有更高的亲和力,具有更强的抗雌激素作用,类雌激素样作用较轻微。托瑞米芬常被用于代替他莫昔芬。托瑞米芬导致子宫内膜病变的发生率低于 TAM,但临床使用中发现,子宫内膜增厚、阴道流血等症状仍有发生,因此,应用本药治疗仍需监测其对子宫内膜的影响。 目前在国内的说明书适应症是用于预防和治疗绝经后妇女的骨质疏松症。FDA 批准适应症是用于降低绝经后妇女骨质疏松症患者或浸润性乳腺癌高危人群浸润性乳腺癌的发生风险。 作用机制:可通过与雌激素受体结合,导致受体主要功能基团失活,同时引起雌激素受体降解及信号通路的阻断,引起雌激素、孕激素受体在细胞水平的表达急剧减少,阻止或延缓内分泌治疗的耐药。 氟维司群:是近年来发现的一类新型甾体类雌激素受体拮抗剂,TAM或AI治疗失败后绝经后晚期乳腺癌一线标准内分泌治疗药物。氟维司群较三苯氧胺能更强地抑制乳腺癌细胞生长,而且无三苯氧胺的弱雌激素作用。氟维司群的副作用包括注射部分反应、虚弱、肝酶升高、恶心、潮热、呕吐、腹泻、皮疹等。 代表药物:戈舍瑞林、亮丙瑞林 作用机制:通过对垂体持续刺激,抑制垂体分泌促卵泡激素(FSH)和促黄体激素(LH),从而达到下调雌激素水平的目的。 是一种合成的、促黄体生成素释放激素的类似物,是一种高效、毒副作用小的药物,是绝经前乳腺癌患者的较佳选择。对绝经前激素受体阳性的早期乳腺癌中危和高危患者推荐OFS联合AI治疗,OFS联合SERM治疗也是合理的选择。对存在SERM禁忌证的任何风险级别的患者,推荐OFS联合AI治疗。戈舍瑞林的副作用包括潮红、皮疹、失眠、骨骼疼痛、盗汗等。年轻女性患者应在接受本品治疗前几个月监测雌激素水平,确保达到绝经状态。 临床应用参考戈舍瑞林。若使用戈舍瑞林后激素水平仍未降至绝经,可更换为亮丙瑞林。亮丙瑞林的副作用:潮热、肩部僵硬、头痛、失眠、眩晕、盗汗、关节痛等。 代表药物:来曲唑,阿那曲唑,依西美坦 作用机制:芳香化酶在人体内,能够催化雄激素向雌激素转化,是绝经后女性体内雌激素的主要来源。芳香化酶抑制剂可以抑制芳香化酶的功能,减少转化而来的雌激素,进一步降低血液中的雌激素水平。 是迄今活性极高、选择性极强的第3代芳香化酶抑制剂非甾体类药物。它在效果、安全性上的优越性已经为多项临床研究所证实。适用于所有绝经后的 ER 和(或)PR 阳性患者。来曲唑不影响肾上腺皮质功能和甲状腺功能,与年龄、肝肾功能没有相关关系,因此老年患者和肝肾功能受损的患者都不必调整剂量。
一、选择性ER调节剂(SERM)
Tamoxifen/ target=_blank class=infotextkey>他莫昔芬:即三苯氧胺
托瑞米芬
雷洛昔芬
二、选择性ER下调剂(SERD)
代表药物:氟维司群
三、卵巢功能抑制剂(OFS)
戈舍瑞林
亮丙瑞林
四、 芳香化酶抑制剂(AI)
来曲唑
阿那曲唑
是强效非甾体类第3代芳香化酶抑制剂,可抑制体内雌激素的转化,降低血浆内雌激素水平,达到抑制乳腺癌生长的目的。经他莫昔芬及其它抗雌激素疗法仍不能控制的绝经后妇女的晚期乳腺癌;绝经后妇女雌激素阳性的早期乳腺癌的辅助治疗;对雌激素受体阴性的病人,若对他莫昔芬呈现阳性的临床反应,可考虑使用阿那曲唑。
依西美坦
第3代芳香化酶抑制剂甾体类药物,主要用于绝经后女性晚期乳腺癌的治疗,通过不可逆地与芳香化酶的活性位点结合,从而使其失活,降低体内雌激素水平,从而达到治疗的目的。
依西美坦抑制更为彻底。部分使用来曲唑、阿那曲唑进展的激素受体阳性的乳腺癌,换用依西美坦治疗后,可能存在一定的效果。
五、CDK4/6抑制剂
代表药物:Palbociclib/ target=_blank class=infotextkey>哌柏西利、阿贝西利
作用机制:通过阻断细胞周期中G1期到S期的进程来抑制ER阳性乳腺癌细胞的增殖。
Palbociclib/ target=_blank class=infotextkey>哌柏西利
是全球首个CDK4/6抑制剂。它曾获美国FDA突破性疗法认定,并已先后于2015年和2018年在美国和中国获批上市。用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌;与芳香化酶抑制剂联合使用作为绝经后女性患者的初始内分泌治疗;用于治疗晚期乳腺癌。哌柏西利的副作用包括感染、血液毒性、食欲下降、口腔炎、腹泻、恶心、呕吐、皮疹、脱发、疲劳、肝功能异常等。
阿贝西利
临床应用参考哌柏西利。联合氟维司群用于二线治疗时,阿贝西利客观缓解率高于哌柏西利。另外,阿贝西利血液系统毒性更少见,腹泻更常见且更严重。
六、组蛋白去乙酰化酶抑制剂
代表药物:西达本胺
作用机制:通过抑制组蛋白去乙酰化酶的活性,提高组蛋白的乙酰化水平引发染色质重塑,改变肿瘤发生的多条信号通路的基因表达,促进肿瘤细胞生长停滞、分化及凋亡。
西达本胺
具有对肿瘤异常表观遗传功能的调控作用。芳香化酶抑制剂(AI)+ 西达本胺作为激素受体阳性(HR+)绝经后晚期患者经他莫昔芬治疗失败后的 I 类推荐,将甾体类 AI+西达本胺作为激素受体阳性(HR+)绝经后晚期患者经非甾体类 AI 治疗失败后的 I 类推荐,证据级别均为 1A 类。西达本胺的副作用包括血液毒性、乏力、发热、腹泻、恶心、呕吐、食欲下降、头晕等。
七、mTOR抑制剂
代表药物:依维莫司
作用机制:可抑制mTOR信号通路,阻断各种生长因子的信号传导,抑制肿瘤生长。
依维莫司
于2012年获批,适用于激素受体阳性复发转移性乳腺癌,及PIK3CA 基因突变的其他分型复发转移性乳腺癌。依维莫司的副作用包括口腔炎、感染、虚弱、乏力、咳嗽、腹泻等。
八、性激素类药物
代表药物:甲地孕酮
作用机制:通过负反馈作用抑制卵泡刺激素和黄体激素的分泌,减少卵巢雌激素的产生,通过抑制促肾上腺皮质激素的分泌,减少肾上腺皮质中雌激素的产生;与孕激素受体(PR)结合后竞争性抑制雌二醇与ER的结合,阻断了雌激素对乳腺癌细胞的作用。
甲地孕酮
可用于晚期乳腺癌的姑息性治疗,并可改善晚期肿瘤患者的食欲和恶病质。副作用主要是肥胖、体液潴留、高血糖和高血压等。
从传统的他莫昔芬、芳香化酶抑制剂、氟维司群,到新研发的CDK4/6抑制剂、mTOR抑制剂以及HDAC抑制剂等,乳腺癌内分泌治疗逐渐向更加多样化、多元化发展。不管是单药治疗,还是联合用药、序贯治疗,只有通过合理选择、有序安排、全程管理和精准决策,才能把每一个优效方案用到最佳!